Chercheurs du réseau CoVaRR-Net
Louis Flamand, Université Laval, directeur du Pilier 3 et chef de projet
Stephen Barr, Université Western, adjoint du Pilier 3
Jenn Corcoran, Université de Calgary, adjointe du Pilier 3
Darryl Falzarano, Vaccine and Infectious Disease Organization (VIDO), adjoint du Pilier 3
Denis Leclerc, Université Laval, adjoint du Piler 3
Silvia Vidal, Université McGill, adjointe du Pilier 3
Jenn Gommerman, Université de Toronto, directrice du Pilier 1
Anne-Claude Gingras, Sinai Health Systems, directrice du Pilier 4
Ioannis Ragoussis, Université McGill, directeur du Pilier 5
Jesse Shapiro, Université McGill, adjoint du Pilier 6
Marc-André Langlois, Université d’Ottawa, directeur général
Résumé simplifié
Malgré l’abondance d’information, il reste beaucoup à apprendre sur la pathogenèse (le processus par lequel une maladie ou un trouble se développe) du SRAS-CoV-2 et de ses variants. La façon dont le SRAS-CoV-2 se transforme en COVID-19 est complexe, mal comprise et comporte de multiples facteurs. On pense qu’elle est probablement en partie le résultat d’une inflammation exagérée et de réponses de coagulation. Une meilleure compréhension de la manière dont le virus évolue en maladie aiderait à optimiser les vaccins. Il est important de continuer à améliorer les vaccins, car les vaccins actuels pourraient être moins efficaces pour contrôler les variants préoccupants (VP), qui se répandent rapidement dans le monde, y compris ici au Canada. Mieux comprendre comment le virus se développe et se renforce aidera également les décideurs canadiens à réagir rapidement aux variants.
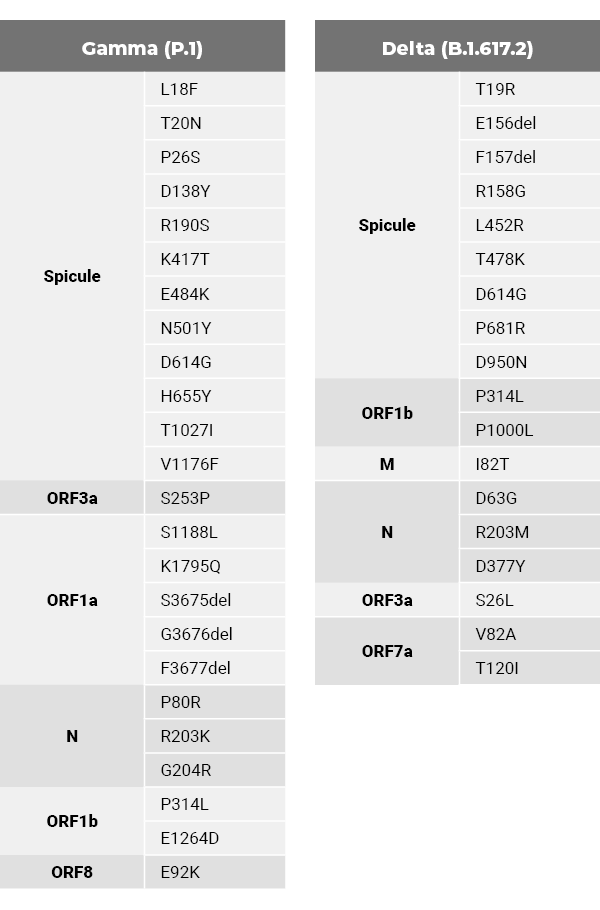
Certaines mutations trouvées dans les variants, comme D614G et N501Y dans le gène du spicule, augmentent la transmissibilité et la virulence du virus. La plupart des études se sont concentrées sur les mutations du spicule, car elles peuvent influencer la protection immunitaire générée par les vaccins actuels. Cependant, les VP contiennent des mutations dans de nombreux autres gènes et on ignore si ces mutations affectent le développement de l’immunité ou la virulence du virus.
Ce projet se concentrera sur les variants Gamma et Delta (voir tableau), étant donné qu’ils semblent être les plus problématiques à l’heure actuelle. Le projet a trois objectifs :
1) Valeur adaptative, pathogenèse et échappement immunitaire des VP développés in vitro et in vivo. Cette partie du projet utilisera la génétique inverse pour aider à a) comprendre l’impact de certaines mutations sur la croissance et la valeur adaptative du VP b) anticiper la façon dont le virus évoluera et se renforcera au Canada en créant une version à mutation rapide du virus pour étudier un processus d’évolution accéléré du SRAS-CoV-2. L’évolution du VP Delta sera également étudiée chez des souris.
2) Modèles animaux pour étudier la pathogenèse du SRAS-CoV-2 et les corrélats de protection. Cette partie du projet étudiera le lien entre les facteurs génétiques de l’hôte, les comorbidités, telles que l’hypertension, et la forme grave de la COVID-19. Les chercheurs compareront la capacité des vaccins et des traitements à protéger contre la forme grave de la COVID-19 et s’efforcer d’établir des liens entre les symptômes et les résultats.
3) La maturation des anticorps et la protection induite par le vaccin contre les VP. Ce segment du projet étudiera les effets des vaccins sur les petits animaux présentant les variants Alpha et Delta. Les chercheurs étudieront l’ensemble de la réponse anticorps afin de déterminer si l’immunité induite par le vaccin augmente avec le temps et si elle protège contre d’autres variants.
Budget
CoVaRR-Net : Contribution en argent de 200 000 $
Tableau des mutations non synonymes dans chaque gène des VOCs Gamma et Delta